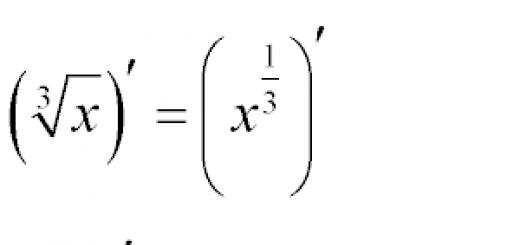Еще алхимики пытались найти закон природы, на основе которого можно было бы систематизировать химические элементы. Но им недоставало надежных и подробных сведений об элементах. К середине XIX в. знаний о химических элементах стало достаточно, а число элементов возросло настолько, что в науке возникла естественная потребность в их классификации. Первые попытки классификации элементов на металлы и неметаллы оказались несостоятельными. Предшественники Д.И.Менделеева (И. В. Деберейнер, Дж. А. Ньюлендс, Л. Ю. Мейер) многое сделали для подготовки открытия периодического закона, но не смогли постичь истину. Дмитрий Иванович установил связь между массой элементов и их свойствами.
Дмитрий Иванович родился в г. Тобольске. Он был семнадцатым ребенком в семье. Закончив в родном городе гимназию, Дмитрий Иванович поступил в Санкт-Петербурге в Главный педагогический институт, после окончания которого с золотой медалью уехал на два года в научную командировку за границу. После возвращения его пригласили в Петербургский университет. Приступая к чтению лекций по химии, Менделеев не нашел ничего, что можно было бы рекомендовать студентам в качестве учебного пособия. И он решил написать новую книгу – «Основы химии».
Открытию периодического закона предшествовало 15 лет напряженной работы. 1 марта 1869 г. Дмитрий Иванович предполагал выехать из Петербурга в губернии по делам.
Периодический закон был открыт на основе характеристики атома – относительной атомной массы .
Менделеев расположил химические элементы в порядке возрастания их атомных масс и заметил, что свойства элементов повторяются через определенный промежуток – период, Дмитрий Иванович расположил периодыдруг под другом., так, чтобы сходные элементы располагались друг под другом – на одной вертикали, так была построена периодическая система элементов.
1 марта 1869г. Формулировка периодического закона Д.И. Менделеева.
Свойства простых веществ, а также формы и свойства соединений элементов находятся в периодической зависимости от величины атомных весов элементов.
К сожалению,
сторонников периодического закона сначала было очень мало, даже среди русских
ученых. Противников – много, особенно в Германии и Англии.
Открытие периодического закона – это блестящий образец научного предвидения: в
1870 г. Дмитрий Иванович предсказал существование трех еще неизвестных тогда
элементов, которые назвал экасилицием, экаалюминием и экабором. Он сумел
правильно предсказать и важнейшие свойства новых элементов. И вот через 5 лет,
в 1875 г., французский ученый П.Э. Лекок де Буабодран, ничего не знавший о
работах Дмитрия Ивановича, открыл новый металл, назвав его галлием. По ряду
свойств и способу открытия галлий совпадал с экаалюминием, предсказанным
Менделеевым. Но его вес оказался меньше предсказанного. Несмотря на это,
Дмитрий Иванович послал во Францию письмо, настаивая на своем предсказании.
Ученый мир был ошеломлен тем, что предсказание Менделеевым свойств экаалюминия
оказалось таким точным. С этого момента периодический закон начинает
утверждаться в химии.
В 1879 г. Л. Нильсон в Швеции открыл скандий, в котором воплотился
предсказанный Дмитрием Ивановичем экабор
.
В 1886 г. К. Винклер в Германии открыл германий, который оказался
экасилицием
.
Но гениальность Дмитрия Ивановича Менделеева и его открытия - не только эти предсказания!
В четырёх местах периодической системы Д. И. Менделеев расположил элементы не в порядке возрастания атомных масс:
Ещё в конце 19 века Д.И. Менделеев писал, что, по-видимому, атом состоит из других более мелких частиц. После его смерти в 1907 г. было доказано, что атом состоит из элементарных частиц. Теория строения атома подтвердила правотуМенделеева, перестановки данных элементов не в соответствии с ростом атомных масс полностью оправданы.
Современная формулировка периодического закона.
Свойства
химических элементов и их соединений находятся в периодической зависимости от
величины заряда ядер их атомов, выражающейся в периодической повторяемости
структуры внешней валентной электронной оболочки.
И вот спустя
более 130 лет после открытия периодического закона мы можем вернуться к словам
Дмитрия Ивановича, взятым в качестве девиза нашего урока: «Периодическому
закону будущее не грозит разрушением, а только надстройка и развитие
обещаются». Сколько химических элементов открыто на данный момент? И это далеко
не предел.
Графическим изображением периодического закона является периодическая система химических элементов. Это краткий конспект всей химии элементов и их соединений.
Изменения свойств в периодической системе с ростом величины атомных весов в периоде (слева направо):
1. Металлические свойства уменьшаются
2. Неметаллические свойства возрастают
3. Свойства высших оксидов и гидроксидов изменяются от основных через амфотерные к кислотным.
4. Валентность элементов в формулах высших оксидов возрастает от I до VII , а в формулах летучих водородных соединений уменьшается от IV до I .
Основные принципы построения периодической системы.|
Признак сравнения |
Д.И.Менделеев |
|
1. Как устанавливается последовательность элементов по номерам? (Что положено в основу п.с.?) |
Элементы расставлены в порядке увеличения их относительных атомных масс. При этом есть исключения. Ar – K, Co – Ni, Te – I, Th - Pa |
|
2. Принцип объединения элементов в группы. |
Качественный признак. Сходство свойств простых веществ и однотипных сложных. |
|
3. Принцип объединения элементов в периоды. |
ЗАНЯТИЕ 5 10-й класс (первый год обучения)
Периодический закон и система химических элементов д.И.Менделеева План
1. История открытия периодического закона и системы химических элементов Д.И.Менделеева.
2. Периодический закон в формулировке Д.И.Менделеева.
3. Современная формулировка периодического закона.
4. Значение периодического закона и системы химических элементов Д.И.Менделеева.
5. Периодическая система химических элементов – графическое отражение периодического закона. Строение периодической системы: периоды, группы, подгруппы.
6. Зависимость свойств химических элементов от строения их атомов.
1 марта (по новому стилю) 1869 г. считается датой открытия одного из важнейших законов химии – периодического закона. В середине XIX в. было известно 63 химических элемента, и возникла потребность в их классификации. Попытки такой классификации предпринимали многие ученые (У.Одлинг и Дж.А.Р.Ньюлендс, Ж.Б.А.Дюма и А.Э.Шанкуртуа, И.В.Деберейнер и Л.Ю.Мейер), но лишь Д.И.Менделееву удалось увидеть определенную закономерность, расположив элементы в порядке возрастания их атомных масс. Эта закономерность имеет периодический характер, поэтому Менделеев сформулировал открытый им закон следующим образом: свойства элементов, а также формы и свойства их соединений находятся в периодической зависимости от величины атомной массы элемента.
В системе химических элементов, предложенной Менделеевым, был ряд противоречий, которые сам автор периодического закона устранить не смог (аргон–калий, теллур–йод, кобальт–никель). Лишь в начале XX в., после открытия строения атома, был объяснен физический смысл периодического закона и появилась его современная формулировка: свойства элементов, а также формы и свойства их соединений находятся в периодической зависимости от величины заряда ядер их атомов.Такую формулировку подтверждает и наличие изотопов, химические свойства которых одинаковы, хотя атомные массы различны.
Периодический закон – один из основных законов природы и важнейший закон химии. С открытия этого закона начинается современный этап развития химической науки. Хотя физический смысл периодического закона стал понятен только после создания теории строения атома, сама эта теория развивалась на основе периодического закона и системы химических элементов. Закон помогает ученым создавать новые химические элементы и новые соединения элементов, получать вещества с нужными свойствами. Сам Менделеев предсказал существование 12 элементов, которые в то время еще не были открыты, и определил их положение в периодической системе. Свойства трех из этих элементов он подробно описал, и при жизни ученого эти элементы были открыты («экабор» – галлий, «экаалюминий» – скандий, «экасилиций» – германий). Кроме того, периодический закон имеет большое философское значение, подтверждая наиболее общие законы развития природы.
Графическим отражением периодического закона является периодическая система химических элементов Менделеева. Существует несколько форм периодической системы (короткая, длинная, лестничная (предложена Н.Бором), спиралеобразная). В России наибольшее распространение получила короткая форма. Современная периодическая система содержит 110 открытых на сегодняшний день химических элементов, каждый из которых занимает определенное место, имеет свой порядковый номер и название. В таблице выделяют горизонтальные ряды – периоды (1–3 – малые, состоят из одного ряда; 4–6 – большие, состоят из двух рядов; 7-й период – незавершенный). Кроме периодов выделяют вертикальные ряды – группы, каждая из которых подразделяется на две подгруппы (главную – а и побочную – б). Побочные подгруппы содержат элементы только больших периодов, все они проявляют металлические свойства. Элементы одной подгруппы имеют одинаковое строение внешних электронных оболочек, что обусловливает их схожие химические свойства.
Период – это последовательность элементов (от щелочного металла до инертного газа), атомы которых имеют одинаковое число энергетических уровней, равное номеру периода.
Главная подгруппа – это вертикальный ряд элементов, атомы которых имеют одинаковое число электронов на внешнем энергетическом уровне. Это число равно номеру группы (кроме водорода и гелия).
Все элементы в периодической системе разделяются на 4 электронных семейства (s -, p -, d -, f -элементы) в зависимости от того, какой подуровень в атоме элемента заполняется последним.
Побочная подгруппа – это вертикальный ряд d -элементов, имеющих одинаковое суммарное число электронов на d -подуровне предвнешнего слоя и s -подуровне внешнего слоя. Это число обычно равно номеру группы.
Важнейшими свойствами химических элементов являются металличность и неметалличность.
Металличность – это способность атомов химического элемента отдавать электроны. Количественной характеристикой металличности является энергия ионизации.
Энергия ионизации атома – это количество энергии, которое необходимо для отрыва электрона от атома элемента, т. е. для превращения атома в катион. Чем меньше энергия ионизации, тем легче атом отдает электрон, тем сильнее металлические свойства элемента.
Неметалличность – это способность атомов химического элемента присоединять электроны. Количественной характеристикой неметалличности является сродство к электрону.
Сродство к электрону – это энергия, которая выделяется при присоединении электрона к нейтральному атому, т. е. при превращении атома в анион. Чем больше сродство к электрону, тем легче атом присоединяет электрон, тем сильнее неметаллические свойства элемента.
Универсальной характеристикой металличности и неметалличности является электроотрицательность (ЭО) элемента.
ЭО элемента характеризует способность его атомов притягивать к себе электроны, которые участвуют в образовании химических связей с другими атомами в молекуле.
Чем больше металличность, тем меньше ЭО.
Чем больше неметалличность, тем больше ЭО.
При определении значений относительной ЭО по шкале Полинга за единицу принята ЭО атома лития (ЭО(Li) = 1); самым электроотрицательным элементом является фтор (ЭО(F) = 4).
В малых периодах от щелочного металла к инертному газу:
Заряд ядер атомов увеличивается;
Число энергетических уровней не изменяется;
Число электронов на внешнем уровне увеличивается от 1 до 8;
Радиус атомов уменьшается;
Прочность связи электронов внешнего слоя с ядром увеличивается;
Энергия ионизации увеличивается;
Сродство к электрону увеличивается;
ЭО увеличивается;
Металличность элементов уменьшается;
Неметалличность элементов увеличивается.
Все d -элементы данного периода похожи по своим свойствам – все они являются металлами, имеют мало различающиеся радиусы атомов и значения ЭО, поскольку содержат одинаковое число электронов на внешнем уровне (например, в 4-м периоде – кроме Cr и Cu).
В главных подгруппах сверху вниз:
Число энергетических уровней в атоме увеличивается;
Число электронов на внешнем уровне одинаково;
Радиус атомов увеличивается;
Прочность связи электронов внешнего уровня с ядром уменьшается;
Энергия ионизации уменьшается;
Сродство к электрону уменьшается;
ЭО уменьшается;
Металличность элементов увеличивается;
Неметалличность элементов уменьшается.
Первый вариант Периодической таблицы элементов был опубликован Дмитрием Ивановичем Менделеевым в 1869 году и назывался «Опыт системы элементов».
Д.И. Менделеев расположил 63 известных в то время элемента в порядке возрастания их атомных масс и получил естественный ряд химических элементов , в котором он обнаружил периодическую повторяемость химических свойств. Данный ряд химических элементов теперь известен как Периодический закон (формулировка Д.И. Менделеева):
Свойства простых тел, а также формы и свойства соединений элементов находятся в периодической зависимости от величины атомных весов элементов.
Современная формулировка закона звучит так:
с войства химических элементов, простых веществ, а также состав и свойства соединений находятся в периодической зависимости от значений зарядов ядер атомов.
Графическим изображением периодического закона является периодическая таблица .

В ячейке каждого элемента указаны его важнейшие характеристики.

Периодическая таблица содержит группы и периоды.
Группа - столбец периодической системы, в котором располагаются химические элементы, обладающие химическим сходством вследствие идентичных электронных конфигураций валентного слоя.
Периодическая система Д.И. Менделеева содержит восемь групп элементов. Каждая группа состоит их двух подгрупп: главной (а) и побочной (б). В главной подгруппе содержатся s- и p- элементы, в побочной - d- элементы.
Названия групп:
I-a Щелочные металлы.
II-a Щелочноземельные металлы.
V-a Пниктогены.
VI-a Халькогены.
VII-a Галогены.
VIII-a Благородные (инертные) газы.
Период - это последовательность элементов, записанная в виде строки, расположенных в порядке увеличения зарядов их ядер. Номер периода соответсвует количеству электронных уровней в атоме.
Период начинается с щелочного металла (или водорода) и заканчивается благородным газом.
|
Параметр |
По группе вниз |
По периоду вправо |
|
Заряд ядра |
Увеличивается |
Увеличивается |
|
Число валентных электронов |
Не меняется |
Увеличивается |
|
Число энергетических уровней |
Увеличивается |
Не меняется |
|
Радиус атома |
Увеличивается |
Уменьшается |
|
Электроотрицательность |
Уменьшается |
Увеличивается |
|
Металлические свойства |
Увеличиваются |
Уменьшаются |
|
Степень окисления в высшем оксиде |
Не меняется |
Увеличивается |
|
Степень окисления в водородных соединениях (для элементов IV-VII групп) |
Не меняется |
Увеличивается |

Современная периодическая таблица химических элементов Менделеева.

Периодический закон Д.И Менделеева.
Свойства химических элементов, а потому и свойства образуемых ими простых и сложных тел, стоят в периодической зависимости, от величины атомного веса.
Физический смысл периодического закона.
Физический смысл периодического закона заключается в периодичном изменении свойств элементов, в результате периодически повторяющихся e-ых оболочек атомов, при последовательном возрастании n.
Современная формулировка ПЗ Д.И Менделеева.
Свойство химических элементов, а также свойство образованных ими простых или сложных веществ находится в периодичной зависимости от величины заряда ядер их атомов.
Периодическая система элементов.
Периодическая система – система классификаций химических элементов, созданная на основе периодического закона. Периодическая система – устанавливает связи между химическими элементами отражающие их сходства и различия.
Периодическая таблица(существует два вида: короткая и длинная) элементов.
Периодическая таблица элементов – графическое отображение периодической системы элементов, состоит из 7 периодов и 8 групп.
Вопрос 10
Периодическая система и строение электронных оболочек атомов элементов.
В дальнейшем было установлено, что не только порядковый номер элемента имеет глубокий физический смысл, но и другие понятия, ранее рассмотренные ранее также постепенно приобретали физический смысл. Например, номер группы, указывая на высшую валентность элемента, выявляет тем самым максимальное число электронов атома того или иного элемента, которое может участвовать в образовании химической связи.
Номер периода, в свою очередь, оказался связанным с числом энергетических уровней, имеющихся в электронной оболочке атома элемента данного периода.
Таким образом, например, „координаты" олова Sn (порядковый номер 50, 5 период, главная подгруппа IV группы), означают, что электронов в атоме олова 50, распределены они на 5 энергетических уровнях, валентными являются лишь 4 электрона.
Физический смысл нахождения элементов в подгруппах различных категорий чрезвычайно важен. Оказывается, что у элементов, расположенных в подгруппах I категории, очередной (последний) электрон располагается на s-подуровне внешнего уровня. Эти элементы относят к электронному семейству. У атомов элементов, расположенных в подгруппах II категории, очередной электрон располагается на р-подуровне внешнего уровня. Это, элементы электронного семейства „р". Так, очередной 50-й электрон у атомов олова располагается на р-подуровне внешнего, т. е. 5-го энергетического уровня.
У атомов элементов подгрупп III категории очередной электрон располагается на d-подуровне , но уже пред внешнего уровня, это элементы электронного семейства «d». У атомов лантаноидов и актиноидов очередной электрон располагается на f-подуровне, пред пред внешнего уровня. Это элементы электронного семейства «f».
Не случайно, следовательно, отмеченные выше числа подгрупп этих 4-х категорий, то есть 2-6-10-14, совпадают с максимальными числами электронов на подуровнях s-p-d-f.
Но можно, оказывается, решить вопрос о порядке заполнения электронной оболочки и вывести электронную формулу для атома любого элемента и на основе периодической системы, которая с достаточной ясностью указывает уровень и подуровень каждого очередного электрона. Периодическая система указывает и на размещение одного за другим элементов по периодам, группам, подгруппам и на распределение их электронов по уровням и подуровням, потому что каждому элементу соответствует свой собственный, характеризующий его последний электрон. В качестве примера разберем составление электронной формулы для атома элемента циркония (Zr). Периодическая система дает показатели и „координаты" этого элемента: порядковый номер 40, период 5, группа IV, побочная подгруппа. Первые выводы: а) всех электронов 40, б) эти 40 электронов распределены на пяти энергетических уровнях; в) из 40 электронов только 4 являются валентными, г) очередной 40-й электрон поступил на d-подуровень пред внешнего, т. е. четвертого энергетического уровня. Подобные выводы можно сделать о каждом из 39 элементов, предшествующих цирконию, только показатели и координаты будут каждый раз иными.
Периодический закон химических элементов - фундаментальный закон природы, отражающий периодическое изменение свойств химических элементов по мере увеличения зарядов ядер их атомов. Открыт 1 марта (17 февраля по ст. стилю) 1869 г. Д.И. Менделеевым. В этот день им была составлена таблица, названная «Опыт системы элементов, основанной на их атомном весе и химическом сходстве». Окончательная формулировка периодического закона была дана Менделеевым в июле 1871 г. Она гласила:
«Свойства элементов, а потому и свойства образуемых ими простых и сложных тел, стоят в периодической зависимости от их атомного веса ».
Менделеевская формулировка периодического закона просуществовала в науке 40 с небольшим лет. Она была пересмотрена благодаря выдающимся достижениям физики, главным образом разработке ядерной модели атома (см. Атом). Оказалось, заряд ядра атома (Z) численно равен порядковому номеру соответствующего элемента в периодической системе, а заполнение электронных оболочек и подоболочек атомов в зависимости от Z происходит таким образом, что сходные электронные конфигурации атомов периодически повторяются (см. Периодическая система химических элементов). Поэтому современная формулировка периодического закона такова: свойства элементов, простых веществ и их соединений находятся в периодической зависимости от зарядов ядер атомов.
В отличие от других фундаментальных законов природы, например таких, как закон всемирного тяготения или закон эквивалентности массы и энергии, периодический закон не может быть записан в виде какого-либо общего уравнения или формулы. Его наглядным отражением является периодическая система элементов. Однако и сам Менделеев, и другие ученые делали попытки отыскать математическое уравнение периодического закона химических элементов
. Эти попытки увенчались успехом только после разработки теории строения атома. Но они касаются лишь установления количественной зависимости порядка распределения электронов в оболочках и подоболочках от зарядов ядер атомов.
Так, путем решения уравнения Шредингера можно рассчитать, как распределяются электроны в атомах с различными значениями Z. И поэтому основное уравнение квантовой механики как бы является одним из количественных выражений периодического закона.
Или, например, другое уравнение: Z„, = „+,Z - - (21 + 1)2 - >n,(2t + 1) +
1
+ т„где „+,Z = - (n + 1+ 1)" +
+(+1+ 1. 2к(п+О 1
2 2 6
Несмотря на свою громоздкость, оно не так уж и сложно. Буквы и, 1, т, и m,- это не что иное, как главное, орбитальное, магнитное и спиновое квантовые числа (см. Атом). Уравнение позволяет вычислить, при каком значении Z (порядкового номера элемента) в атоме появляется электрон, состояние которого описывается заданной комбинацией четырех квантовых чисел. Подставляя возможные сочетания и, 1, т, и т, в это уравнение, мы получаем набор различных значений Z. Если эти значения расположить в последовательности натурального ряда чисел 1, 2, 3, 4, 5, ..., то, в свою очередь, получается четкая схема построения электронных конфигураций атомов по мере роста Z. Таким образом, это уравнение - также своеобразное количественное выражение периодического закона. Попробуйте сами решить это уравнение для всех элементов периодической системы (как связаны между собой значения и, 1; m, и т„ вы узнаете из статьи Атом).
Периодический закон - это универсальный закон для всей Вселенной . Он имеет силу везде, где существуют атомы. Но периодически изменяются не только электронные структуры атомов. Строение и свойства атомных ядер также подчиняются своеобразному периодическому закону. В ядрах, состоящих из нейтронов и протонов, существуют нейтронные и протонные оболочки, заполнение которых имеет периодический характер. Известны даже попытки построения периодической системы атомных ядер.